Electronic Data Capture (EDC)-System
Erfassen Sie vollständige, konsistente und sichere Daten in einem EDC-System, das auf die individuellen Bedürfnisse Ihrer klinischen Studie zugeschnitten ist.
Skalierbar, bedienungsfreundlich, integrierbar: Die Software as a Service (SaaS)-Architektur verknüpft Patienten, Sponsoren und Studienzentren nahtlos, um maximale Zeit- und Kostenersparnisse zu erzielen.
Nachfolgend finden Sie eine umfassende Funktions-Übersicht sowie wichtige Informationen zu Electronic Data Capture mit der RAYLYTIC-Plattform.
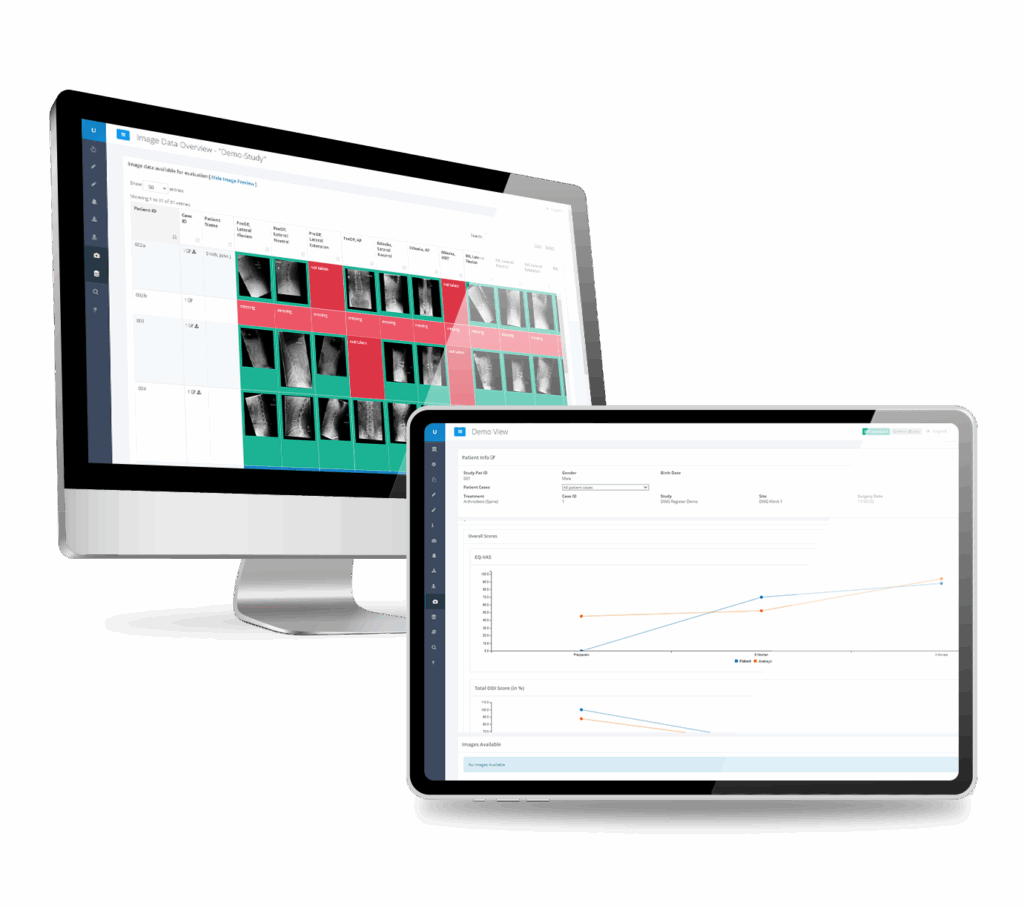
Das einzige EDC-System mit nativer Integration von Bildgebungsdaten
Unsere EDC-Plattform integriert bildgebende eCRFs nativ in die klinische Datenerfassung und eliminiert den manuellen Abgleich, der den Datenbankabschluss verzögert. Erfassen Sie radiografische Bewertungen, Geräteleistungskennzahlen und Patientenergebnisse in einem einzigen System
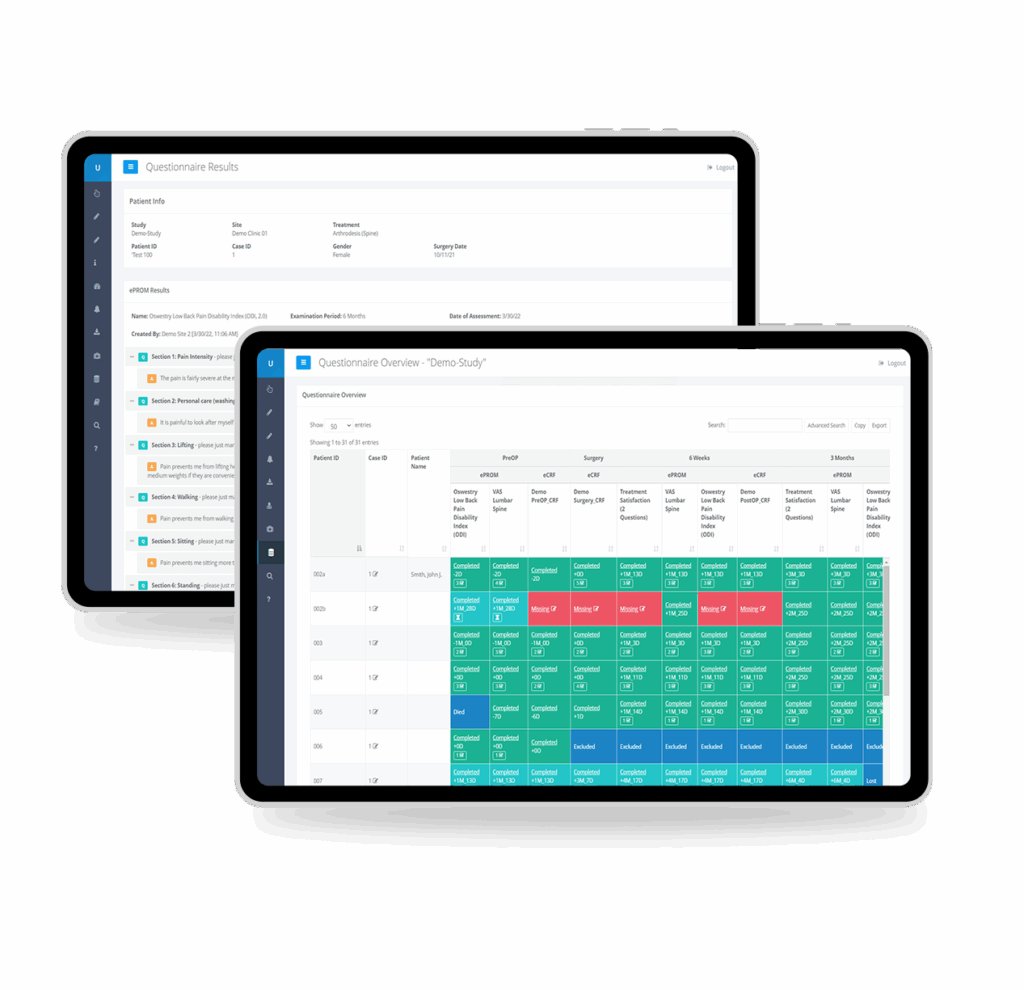
eCRFs
Gestalten Sie flexible eCRFs, die speziell auf Studien mit Medizinprodukten zugeschnitten sind – von Standard-Visite-Formularen bis hin zu gerätespezifischen Bewertungen. Integrierte Bearbeitungsprüfungen, automatische Validierung und intuitive Formulargestaltung gewährleisten eine hochwertige Datenerfassung ohne Programmierkenntnisse.
Bildgebende eCRFs
Speziell entwickelte bildgebende eCRFs erfassen radiografische Bewertungen direkt in Ihrer Studiendatenbank. Die native Integration mit Bildgebungs-Endpunkten eliminiert manuelle Abgleiche, beschleunigt den Datenbankabschluss und stellt sicher, dass Bildgebungsdaten zusammen mit klinischen Daten gespeichert werden – nicht in getrennten Silos.
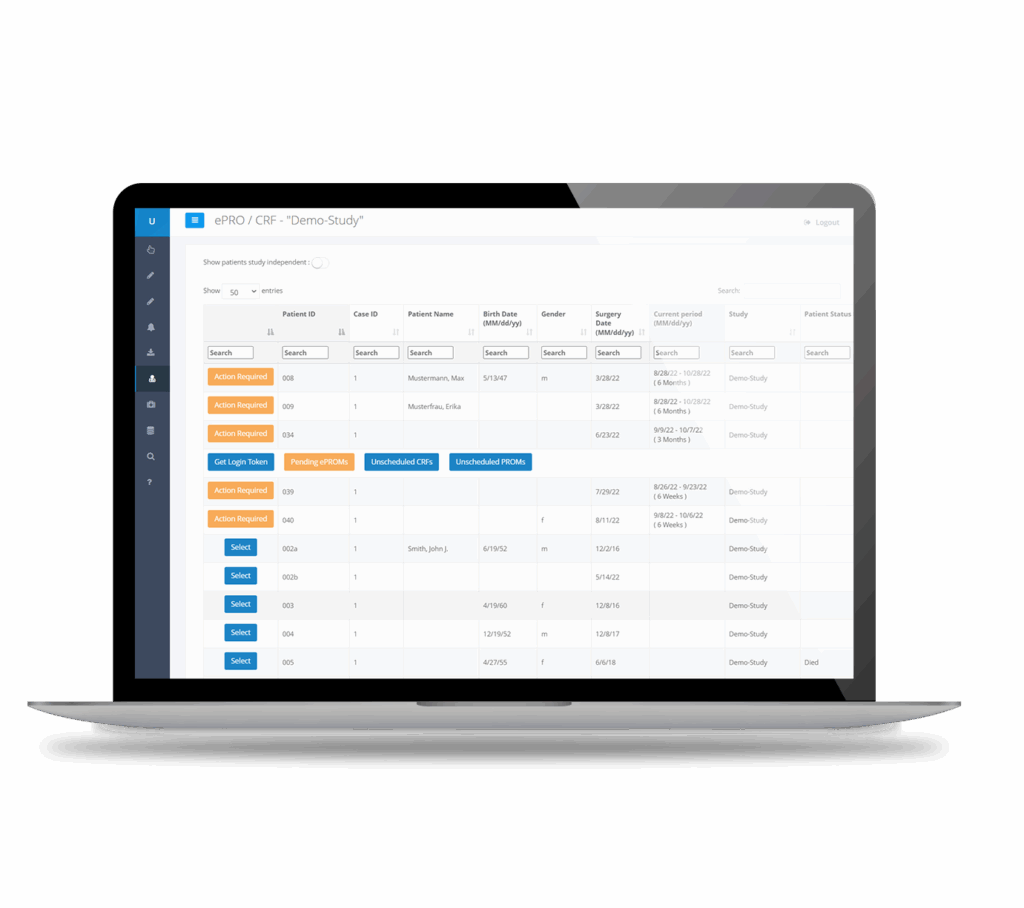
ePROs & PROMs
Vollständige Funktionalität für elektronische patientenberichtete Ergebnisse (ePRO) und patientenberichtete Ergebnismessungen (PROM) mit automatisierter Terminplanung, Fernerfassung von Daten, Echtzeit-Auswertung und sofortiger Visualisierung. Speziell entwickelt für Studien mit Medizinprodukten, bei denen Patientenerfahrung und funktionale Ergebnisse kritische Endpunkte sind.
Individuelle Fragebögen: UE-Formulare & Mehr
Erstellen Sie individuelle Formulare für die Meldung unerwünschter Ereignisse, die Nachverfolgung von Gerätemängeln, Begleitmedikationsprotokolle und alle studiespezifischen Datenerfassungsbedürfnisse. Unser intuitiver Formular-Designer ermöglicht es Ihnen, regulierungskonforme Fragebögen ohne Programmierung zu erstellen – präzise auf Ihre Anforderungen an Studien mit Medizinprodukten zugeschnitten.
Erfassen Sie klinische und Bildgebungsdaten in einem einzigen, regelkonformen EDC-System
Bringen Sie eCRFs, medizinische Bilddaten und Patientenergebnisse (z.B. PROMs) in einer einzigen verlässlichen Plattform zusammen, um manuelle Arbeit, Datensilos und Query-Zyklen zu reduzieren. Ihre Teams verbringen weniger Zeit mit der Verwaltung von Systemen und mehr Zeit mit dem, was zählt: die Verbesserung von Patientenergebnissen und die Beschleunigung des Studienabschlusses
- Anpassbare eCRFs, ePROs, UE-Formulare, ePREMs oder Anamnese-Formulare
- Sponsor-spezifische Fragen zur Protokollierung von Protokollabweichungen in eCRFs
- Ungeplante UE-Fragebögen/Formulare/Protokollabweichungen
- Mehrsprachige Fragebögen ohne Änderungen in der Benutzererfahrung
- Datenbank-Design per Drag-and-Drop
- Self-Service Datenbank- und Protokolländerungen ohne Ausfallzeiten
- Unbegrenzte Datenbankgröße
- Skalierbare Infrastruktur für Bilder von Einzelzentren bis hin zu globalen multizentrischen Studien
- HIPAA-konforme Bild-Upload, -Übertragung und -Speicherung (automatische Anonymisierung von Bilddaten)
- Integrierte eCRF-Erstellung für zentrales Bild-Review
- Strukturierte Bild-Review-Vorlagen, konfiguriert für Ihre spezifischen Studienprotokolle
- Intelligente Bildbewertung zur Unterstützung der Protokoll-Compliance
- Zentralisierte Bilddatenbank mit Multizentren-Zugriff und rollenbasierten Berechtigungen
- Unterstützung für mehrere Bildmodalitäten (CT, MRT, Röntgen, Ultraschall und mehr)
- Integrierte KI-basierte Bildanalyse für ausgewählte radiografische Ergebnisse
- Anpassbare Dashboards und Datenvisualisierungen
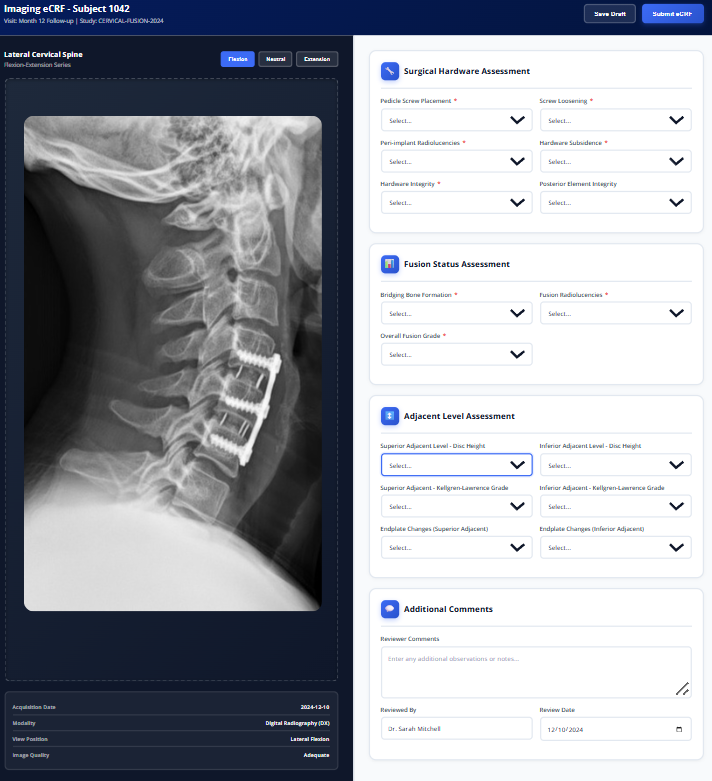
Generieren Sie aussagekräftige Real-World-Evidence in einem flexiblen EDC-System
Unser EDC-System wurde zur digitalen Erfassung von Daten aus den für Ihre Studie wichtigsten Quellen entwickelt.
Sponsorinitiierte Register für die kontinuierliche Erfassung von Real-World-Daten
International akzeptiert durch automatische Sprachanpassungen
Konform mit EU- und US-Datenschutzanforderungen
Integration ins KIS, Terminierungssoftware, Labor- und Archivanwendungen, PACS, usw.
Konfigurierbares Integrationslayer zur Vereinheitlichung von Daten zwischen UNITY und gängigen KIS-Anbietern
Brücke zwischen HL7 v2/v3/CDA und FHIR
Bi-direktionale Schnittstelle
Exporte im neutralen CSV-Format zur einfachen Nutzung durch SAS, Excel oder andere Anwendungen
Profile, Mappings und APIs zur Anpassung an Ihre Anforderungen im Stammdatenmanagement
Fragebogendesigner für frei definierbare eCRFs, PROMs, PREMs und andere Fragebögen
Sponsor-spezifische Fragen zur Erfassung von Protokollabweichungen in eCRFs
Ad-hoc Aufruf und Erstellen von Fragebögen, Protokollabweichungen, Formularen
Mehrsprachige Fragebögen mit intuitiver Benutzeroberfläche
Studiendesign per Drag-and-Drop
Selbstständige Datenbank– und Protokolländerungen ohne Systemunterbrechungen
Dauer des Datenbanksetups dauert durchschnittlich 90 Minuten
Unbegrenzte Datenbankgröße
Verwalten sie multizentrische klinische Studien effizient und ressourcenschonend
Echtzeitberichte, konfigurierbare Benachrichtigungen und umfangreiche Visualisierungen des Studienfortschritts erleichtern Ihnen das Monitoring von großen multizentrischen klinischen Studien.
Automatischer Export von PROM-Daten an Register von Drittanbietern
Analyse und Validierung der Datenqualität in Echtzeit
Ereignis- oder zeitgesteuerte Alarme, Benachrichtigungen, Erinnerungen, Datenübermittlungen und Berichte zur Automatisierung von Verwaltungsaufgaben
Automatisierte Validierung zwischen mehreren Datenfeldern und Datensätzen umfassen
Konfigurierbare E-Mail-Benachrichtigungen nach frei definierbaren Kriterien. Zum Beispiel:
Vorabinformation zu bevorstehenden Fragebögen
Bei bestimmten Formulareingaben
Für definierte Punkte des Studienverlaufs
Für zahlreiche Ereignisse (Einsendung eines Fragebogens, unerwünschte Ereignisse, PROM-Scores, usw.)
Erste Einladung und automatische Erinnerungsmeldungen zur Automatisierung der Kommunikation mit den Patienten
Medizinische Kodierung in MedDRA, RadLex und anderen auf Anfrage
Zuordnung medizinischer Codes zu wörtlichen Begriffen in vorhandenen Daten
Autokodierung, Synonymlisten, automatische Feststellung von Kodierungskonflikten
Dashboards zur Anzeige von Studienfortschritt und Datenstatus
Berichte und Statistiken über die Gesamtzahl der Teilnehmer, die Teilnehmerzahl pro Standort, die Vollständigkeit der Daten und das Auftreten von Meldungen
Terminierung automatisch erstellter Berichte
Ad hoc-Datenexport, Berichte, Queries
Quelldatenverifizierung auf verschiedenen Ebenen (z.B. Eingabefeld, Formular, Patientenebene)
Elektronische Unterschriften von Patienten und Investigatoren / Sponsoren
Anzeige aller offenen und gelösten Queries
Intuitiver Prozess zur Lösung von Queries
Anpassbare Benutzeroberfläche für Patienten durch Sponsor-User
Dateneingabe über Tablet, Computer oder Mobiltelefon
Hochladen von Quell- und Archivierungsdokumenten
Erheben Sie Daten sicher und gesetzeskonform
Die RAYLTIC Plattform ist absolut gesetzeskonform und gewährleistet ein Höchstmaß an Datenschutz. Dabei werden die höchsten wissenschaftlichen und regulatorischen Anforderungen erfüllt.
Das Modul zur Erhebung von PROMs ist ein Medizinprodukt der Klasse I nach Medizinprodukteverordnung (2017/745/EU).
Alle Systeminteraktionen sind im Auditrail komplett protokolliert
Exportierbare Audit-Trails als PDF-Datei
DSGVO-konform
GCP-konform
SaaS Architektur mit ISO 27001 zertifizierten Geschäfts- und Datenspeicherungsprozessen
ISO 13485 Zertifizierung


Wissenswertes zu EDC-Systemen und eCOA
Der Einsatz von elektronischer Datenerfassung (EDC) und elektronische Clinical Outcome Assessment (eCOA) für klinische Studien hat in den letzten zwei Jahrzehnten erheblich zugenommen. Da immer mehr Lösungen auf den Markt kommen, sind die Grenzen zwischen EDC-Systemen, eCOA und PROMs inzwischen fließend. Der Hauptunterschied zwischen EDC und eCOA besteht in der Verantwortung für die Dateneingabe.
Was ist der Unterschied zwischen einem EDC-System und eCOA?
Elektronische Datenerfassung (EDC) und elektronisches Clinical Outcome Assessment (eCOA) sind zwei gängige Begriffe im Kontext klinischer Studien. Oft werden sie synonym verwendet, aber sie stellen tatsächlich zwei verschiedene Methoden der elektronischen Datenerfassung dar.
EDC-Daten
Der Hauptunterschied zwischen EDC und eCOA ist, wer die Daten ins System eingibt. EDC-Daten werden von Studienkoordinatoren oder Datenmanagern ins EDC-System eingebracht. So können diese Daten entweder rein elektronisch erhoben oder z.B. von einem papierbasierten Einzelfallbericht transkribiert werden.
eCOA-Daten
eCOA-Daten hingegen werden direkt von Patienten, Ärzten oder Bezugspersonen über ein mobiles Endgerät, Tablet oder einen Computer ins System eingespeist. Elektronische Patient-Reported Outcome Measures (ePROMs) sind somit eine Form von eCOA. Nachdem eine Patientin z.B. ein PROM ausgefüllt hat, werden die Ergebnisse sofort in die Datenbank eingepflegt – ohne externen Eingriff.
Für Datenmanager ist es essentiell, mit konsistenten und hochwertigen Daten arbeiten zu können, daher sind EDC-Systeme funktionell komplexer als ein Modul zur Erfassung von eCOA-Daten. Der Unterschied in der Komplexität der zwei Systeme lässt sich am Beispiel von Editierprüfungen (engl. edit checks) gut veranschaulichen. Ein EDC-System bietet einer Datenmanagerin vielfältige Möglichkeiten zur Einstellung von Eingabelimitierungen, Datenverifizierungsmaßnahmen oder zum Abgleich von Daten über Fragebögen oder Formulare hinweg.
Editierprüfungen in einem PROM als Teil von einem eCOA-Modul hingegen sind darauf ausgerichtet, die Patientin zum vollständigen Ausfüllen des Fragebogens anzuleiten.
Kurzum bietet ein EDC-System die Möglichkeit, die Konsistenz und Qualität der eCOA-Daten zu überprüfen.
Wie unterscheiden sich eCOA und PROMs?
eCOA ist eine Methode zur elektronischen Erfassung von Daten verschiedener Teilnehmer einer klinischen Studie. Sie dient als Sammelbegriff für alle elektronisch erfassten Ergebnisse. In den letzten 15 Jahren hat sich die Verwendung von eCOA rapide ausgeweitet, da sie eine schnellere Möglichkeit darstellt, strukturierte, saubere Daten zu erfassen und diese Daten in die Studiendatenbank zu integrieren. Heute gibt es viele verschiedene Arten von eCOA, die sich vor allem darin unterscheiden, was der Anlass des Outcomes ist und wer die Daten berichtet:
Electronic Patient-Reported Outcome Measures (ePROMs): Die Patienten berichten über ihre gesundheitsbezogene Lebensqualität, Symptome oder Schmerzen.
Electronic Performance Outcome (ePerfO): Die Patienten berichten über ihre Erfahrungen mit einer körperlichen oder kognitiven Aufgabe.
Electronic Clinician-Reported Outcome (eClinRO): Ergebnisse, die von Klinikern über Patienten berichtet werden.
Electronic Observer-Reported Outcome (eObsRO): Von anderen Betreuungspersonen berichtete Ergebnisse
PROMs als eine Form von eCOA
PROMs sind daher eine Form von eCOA. PROMs sind in der Regel Teil eines größeren eCOA-Moduls, das verschiedenen Beteiligten die Möglichkeit bietet, diverse für die klinische Studie erforderliche Fragebögen auszufüllen. Mit PROMs berichten Patienten über ihre persönliche Wahrnehmung ihrer Behandlung, ihrer Symptome oder ihrer gesundheitsbezogenen Lebensqualität. Als Teil einer klinischen Studie sind PROMs ein patientenorientierter Weg, um die Auswirkungen einer Behandlung zu verstehen.